はじめに
当研究室では、ゲノムから機能的RNAが作り出されるまでの過程―すなわちエピジェネティック制御、転写の開始・伸長・終結、RNAプロセシングという一連の過程―の解明を目指しています。私達の体を構成する1つ1つの細胞は、同一のゲノムを持っているにも関わらず多彩な機能を果たしています。これは、ゲノム情報の発現が時空間的に極めて巧妙に制御されているためです。当研究室では、ゲノム情報発現の過程を制御するタンパク質因子群の同定・解析や、ゲノムから多様なトランスクリプトームが生じるメカニズムの解明を目指した研究を行なっています。こうした地道な基礎研究の積み重ねは、一例を挙げればES細胞がES細胞らしい性質を保持するしくみの解明などに役立ちます。

転写伸長制御のメカニズム
転写反応はまずRNAポリメラーゼがゲノム上の遺伝子領域にリクルートされる開始段階、RNAポリメラーゼが遺伝子領域を5’方向から3’方向へ向かってmRNA合成を進める伸長段階、RNAポリメラーゼが遺伝子の転写を終えてゲノム上から離れる終結段階の3つの段階に分かれています。これらの反応はゲノムDNAやRNAポリメラーゼに結合する様々な因子の働きによって行われています。1990年代に時計の針を戻すと、当時は転写開始段階の研究が真っ盛りで、真核生物における遺伝子発現のオン・オフ制御は転写開始段階こそが重要と広く信じられていました。
そのような状況下で、当研究室はDRBという転写阻害剤に注目しました。DRBはRNAポリメラーゼII転写の特異的阻害剤で、哺乳動物培養細胞に添加すると、長い転写産物の合成が阻害され、短い転写産物が蓄積することが報告されていました。したがって、DRBは転伸長段階を阻害している可能性が考えられましたが、DRBは意外なことに、精製されたRNAポリメラーゼIIを阻害しませんでした。そこで私達は、生化学的アプローチによりDRBの阻害のメカニズム解明を目指しました。
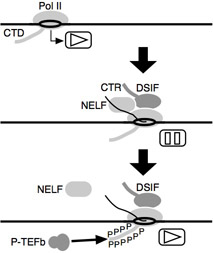 その結果、私達はDSIF(SPT4-SPT5)とNELFという2つの転写伸長因子を新規に同定しました。また、その当時、競っていたDavid Price研が発見したP-TEFbという転写伸長因子が、DSIF、NELFと拮抗的に働くことを突き止めました。すなわち、DSIFとNELFは、転写開始直後のRNAポリメラーゼIIに結合することで、転写伸長を阻害するブレーキ役として働きます。これを解除するのがP-TEFb(CDK9-Cyclin T)です。P-TEFbはタンパク質リン酸化酵素活性をもち、RNAポリメラーゼIIのC末端ドメイン(CTD)や、DSIFのC末端ドメイン(CTR)などをリン酸化することでNELFの脱離を誘導し、転写を再活性化します。このリン酸化をきっかけにして、CTDやCTRに結合するタンパク質因子がさらにリクルートされ、成熟した転写伸長複合体へと変化することが分かってきました。
その結果、私達はDSIF(SPT4-SPT5)とNELFという2つの転写伸長因子を新規に同定しました。また、その当時、競っていたDavid Price研が発見したP-TEFbという転写伸長因子が、DSIF、NELFと拮抗的に働くことを突き止めました。すなわち、DSIFとNELFは、転写開始直後のRNAポリメラーゼIIに結合することで、転写伸長を阻害するブレーキ役として働きます。これを解除するのがP-TEFb(CDK9-Cyclin T)です。P-TEFbはタンパク質リン酸化酵素活性をもち、RNAポリメラーゼIIのC末端ドメイン(CTD)や、DSIFのC末端ドメイン(CTR)などをリン酸化することでNELFの脱離を誘導し、転写を再活性化します。このリン酸化をきっかけにして、CTDやCTRに結合するタンパク質因子がさらにリクルートされ、成熟した転写伸長複合体へと変化することが分かってきました。
これら以外にも多数の転写伸長因子が同定され、転写伸長の研究分野は発展してきました。大学の教科書にも取り上げられるようになり、分野として確立された感はありますが、いまだトップジャーナルに機能解析や構造解析の論文が掲載され、アクティブな研究分野であり続けています。
転写伸長制御の生理学的意義
転写伸長制御のメカニズム研究とは別に、その生理学的意義の解明を目指す研究が並行して行われています。ヒト培養細胞をモデル系として用いて行う研究に加えて、様々なモデル生物を用いて共同研究として進める研究もあります。
転写伸長制御の生理学的意義としてまず明らかなのは、前初期遺伝子(immediate-early genes)と総称されるような、外部からの刺激に応答して素早く発現する遺伝子群の転写誘導に果たす役割です。つまり、mRNAの完成直前の段階でRNAポリメラーゼIIの転写を止め、クロマチンはアクティブな状態に保っておき、いざ外部から刺激が入ったら速やかに転写を再開できるようにする、というのが転写伸長制御の生理学的意義と考えられ、熱ショック、増殖因子、ホルモン等に応答して発現する遺伝子群を対象とした研究で、実際にこのモデルが確かめられてきました。
また、ゼブラフィッシュやショウジョウバエ個体を用いた共同研究により、転写伸長制御が脳神経系の発生・分化に重要な役割を果たしていることも明らかとなってきました。発生・分化過程では、多数の細胞種特異的遺伝子の発現がダイナミックに変動しているので、前初期遺伝子と似た状況が現出していると考えられます。
さらに、近年発展著しい次世代シーケンサーにより、ゲノム全体の情報が詳細に得られるようになりました。それにより、生化学では絶対にアプローチできない、個々の遺伝子上でのRNAポリメラーゼIIや転写因子の振る舞いを調べることが可能になりました。そして実際、DSIFやNELFなどによる転写伸長制御がゲノム発現全体に重要であることが分かってきました。
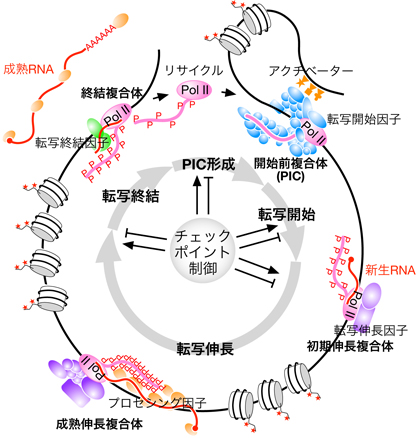
転写終結制御のメカニズム:多様なトランスクリプトームはいかにして生じるのか
当研究室は、転写終結段階の制御によって多様なトランスクリプトームが生じるメカニズムについても積極的に研究しています。RNAポリメラーゼIIが転写する遺伝子には3種類のRNA 3’末端プロセシング経路が存在し、それらが遺伝子によって使い分けられています。また原理上、3’末端プロセシングは転写終結と共役しており、3’末端プロセシングが転写終結を誘導しますが、私達は最近、転写の開始や伸長などに関与すると考えられていた因子(NELF、CBC、Mediator、LECなど)が3種類のプロセシング経路の使い分けにも関与している証拠を得ました。さらに、1つの遺伝子に複数の転写終結点が存在するケースが多々あり、それらの使い分けに関与する因子群についても同定・解析を進めています。同一のゲノムから、細胞種ごとに多様なトランスクリプトームが生じますが、その一端がこうした転写終結段階の制御によって達成されていると考えられます。
私達は次世代シーケンサーを用いたゲノム・トランスクリプトーム解析に加えて、最先端の質量分析装置を用いたプロテオーム解析やCRISPR/Cas9を用いた遺伝学的な手法を組み合わせて、これらの課題に取り組んでいます。そこでは、生命情報学のアプローチが大変重要になります。

はじめに
私達はおよそ60兆個の細胞から成り立っており、その細胞は水分を除けば主に脂質、タンパク質、そして核酸から成り立っています。この極めて高度な機械ともいえる細胞の働きを調節しているのが、無数の低分子化合物(通常、分子量1,000以下)です。ビタミン、ステロイドホルモン、ヘムなどが生体内の低分子化合物として例に挙がります。また日常生活で時折お世話になる医薬品も、その多くは低分子化合物からなっています。しかし、様々な低分子化合物が生体内において分子レベルでどのような影響を及ぼすのか、まだ充分には理解されていません。市販され、我々が使っている医薬品ですら、薬効メカニズムが不明なものが多く存在しています。
複雑な生体システムを理解する上で低分子化合物は極めて有用なツールです。ある化合物が生体に影響するしくみの解明は、標的タンパク質が関与する未知の生体内分子ネットワークの解明に繋がります。さらに用いた化合物が医薬品の場合、こうした知見はドラッグリポジショニングや新薬開発にも繋がります。ケミカルバイオロジーというのは、こうした課題に取り組む学際的な研究分野で、私達は独自の相互作用解析技術(プロテオミクス)や遺伝学的スクリーニング技術を用いて創薬を目指した研究を進めています。
研究手法
研究室独自の手法として、FGビーズを用いた生化学的手法があります。当研究室は2012年3月に退官した半田宏名誉教授の下で、低分子化合物の生体内作用メカニズム解明を目的とした研究ツールの開発にチャレンジし、優れたアフィニティクロマトグラフィー用担体であるFGビーズを開発しました。FGビーズは磁性鉄(Fe3O4)をコアに持つ粒径140〜200nmの微粒子で、興味ある低分子化合物などのリガンドを固定化したFGビーズを用いることで、ワンステップかつ短時間で標的因子を精製できます。このビーズは非常にバックグラウンドが低く、高収率であり、ビーズ自体は化学的にも安定で、表面修飾(カルボン酸やアミノ基などの導入)を比較的容易に行うことができます。また、FGビーズは磁性を有しているので、遠心機を用いず、磁気分離による精製が可能です。FGビーズは製品化にも成功しており、多摩川精機株式会社より購入可能です。私達はFGビーズを用いたケミカルバイオロジー研究により、これまでに様々な低分子化合物が織りなす重要で興味深いメカニズムを明らかにしてきました。
私達はまた、アフィニティクロマトグラフィー法ではアプローチが難しい分子間相互作用を探索・同定する新たな手法として、距離依存性のin situビオチン化法の開発も行なっています。さらに、相互作用ベースのアプローチを相補する機能ベースの遺伝学的アプローチとして、CRISPR/Cas9を用いたsgRNAライブラリースクリーニングも行なっています。
サリドマイド研究と新たな創薬展開
私達の創薬を目指した研究の最大の成果が、サリドマイド標的因子の同定です。サリドマイドは1950年代に催眠・鎮静剤として開発された薬剤ですが、当初見過ごされていた催奇形性を有しており、妊娠初期の女性が服用した結果、手足に奇形を持つ多くの赤ちゃんが誕生しました。このサリドマイド禍は史上最悪の薬害事件の1つとして記憶されています。しかしサリドマイド研究はその後も続けられ、サリドマイドがハンセン病や多発性骨髄腫(血液がんの一種)等に対して非常に優れた治療効果をもつことが判明しました。その結果、今世紀に入ってサリドマイドとその後継薬は世界的によく使われる医薬品としてスポットライトを浴びるようになりました。サリドマイドの作用機構は長らく不明でしたが、私達は2010年、半田宏名誉教授や伊藤拓水博士らとともにFGビーズ技術を用いて、サリドマイドの細胞内標的がセレブロン(CRBN)というタンパク質であることを発見し、この研究領域にブレイクスルーをもたらしました。
サリドマイドとCRBNは、単なる1薬剤-1標的分子の関係性にとどまらず、創薬の新たな基盤となる拡張性・発展性を持っています。CRBNはE3ユビキチンリガーゼ複合体CRL4CRBNの基質を認識するサブユニットで、サリドマイド系薬剤がCRBNに結合すると基質特異性が変化し、本来は基質とならないタンパク質 (ネオ基質)のユビキチン化・分解が誘導されることが分かってきました。つまり、サリドマイド系薬剤はCRL4CRBNとネオ基質とを橋渡しする「分子のり」として働き、様々なネオ基質の分解を誘導することで多様な薬効を発揮していると考えられ、CRBNのネオ基質の探索・同定が近年の重要な研究課題となっています。サリドマイド系薬剤の分子構造を少し変えると、異なるネオ基質のユビキチン化・分解が誘導されることから、分子設計次第で、これまで創薬標的となり得なかったタンパク質を標的とすることが可能で、創薬開発の新たなアプローチとして現在、大変注目されています。
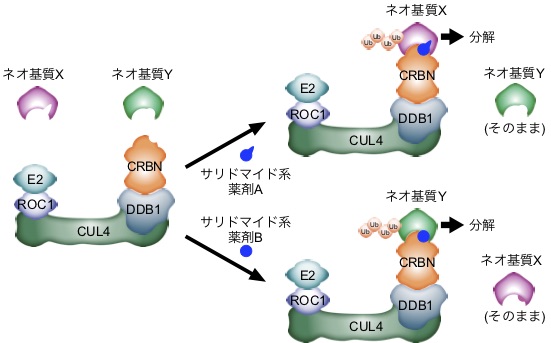
以上のように、サリドマイド系薬剤は大きな可能性を秘めており、私達が精力的に研究している領域でもあります。私達の研究が人々の健康な生活に繋がることを願って研究を続けています。
